مفهوم اصلی
در این آموزش با چهار مورد اصلی آشنا خواهید شد حالات ماده (جامد، مایع، گاز و پلاسما)، و همچنین برخی حالت های میانی ماده، با خواندن خواص، کاربردها و نمونه های آنها.
موضوعات تحت پوشش در مقالات دیگر
واژگان
- میدان مغناطیسی – ناحیه ای در اطراف آهنربا یا جریان الکتریکی که تأثیر مغناطیسی بر بارهای الکتریکی متحرک، جریان ها و مواد مغناطیسی را توصیف می کند. بار الکتریکی متحرک در یک میدان مغناطیسی نیرویی عمود بر سرعت خود را تجربه می کند.
- موضوع– هر چیزی که جرم داشته باشد و فضا را اشغال کند. اتم ها و ترکیباتی را تشکیل می دهد که خواص فیزیکی و شیمیایی را تشکیل می دهند. برای اطلاعات بیشتر در مورد مفهوم ماده، این مقاله را بررسی کنید!
- فاز و موضوع گاهی اوقات به عنوان مترادف استفاده می شود. با این حال، ممکن است چندین فاز تشکیل شود که در یک حالت ماده هستند (مانند اینکه چگونه جامدات می توانند ساختارهای کریستالی متفاوتی داشته باشند).
حالات ماده چیست؟
چهار حالت اصلی ماده وجود دارد که در زندگی روزمره مشاهده می شود: جامد، مایع، گاز و پلاسما. علاوه بر این، بسیاری از حالت های میانی وجود دارد که بسیاری از آنها فقط در شرایط شدید وجود دارند. در کل، 20 وجود دارد! با توجه به تفاوت آنها در ویژگی ها که عوامل متمایز آنها است، اجازه دهید به برخی از حالات ماده در زیر بپردازیم:
مواد جامد
در حالت جامد، ذرات در یک آرایش ثابت در کنار هم قرار می گیرند. به دلیل نیروهای قوی که آنها را در کنار هم نگه میدارند، ذرات یک جامد تنها در ارتعاشات کوچک قادر به حرکت به جلو و عقب هستند. به عبارت دیگر در موقعیت های ثابت خود باقی می مانند. در نتیجه، جامدات کمترین انرژی جنبشی را در بین تمام حالات ماده دارند.
ذرات ترکیب یا به صورت شبکه ای منظم و هندسی یا به شکل تصادفی و بدون ساختار متصل می شوند. مواد موجود و شرایطی که در آن یک جامد ایجاد میشود، تعیین میکند که جامد کریستالی یا آمورف باشد. معمولاً وقتی شرایط ثابت است (مانند سرد شدن/گرمایش تدریجی و آهسته)، ذرات این شانس را دارند که به طور یکنواخت تراز شوند. با این حال، هنگامی که تغییرات شدید و سریع دما وجود دارد، به احتمال زیاد یک جامد با شکل نامحدود نتیجه خواهد بود.
جامدات شکل و حجم مشخصی دارند، یعنی دارای موقعیت ثابت هستند و با شکل ظرف خود مطابقت نخواهند داشت. از آنجایی که ذرات آنها بسیار متراکم هستند، جامدات تمایل به چگالی بالایی دارند و بدون استفاده از نیروی خارجی زیاد به سختی فشرده می شوند.

کلاس های جامدات
چه متوجه باشیم یا نه، انواع مختلفی از مواد جامد در اطراف ما وجود دارد – از نمک غذا گرفته تا صندلی چوبی! از آنجایی که انواع نیروها و پیوند بین ذرات می تواند متفاوت باشد، طبقات مختلفی از جامدات وجود دارد. این کلاس ها شامل فلزات، مواد معدنی، سرامیک (شیشه)، مولکول های آلی، مواد کامپوزیت، نیمه هادی ها، نانومواد و بیومواد می باشد. این دسته از جامدات به دلیل برهمکنشهای نیرویی متفاوت، خواص فیزیکی و شیمیایی متفاوتی دارند. این خواص عبارتند از: خاصیت ارتجاعی، رسانایی، عبور نور، انعطاف پذیری و غیره.
مایعات
در حالت مایع، ذرات آزادی بیشتری برای جریان در اطراف یکدیگر دارند، زیرا آنها شل تر از جامد هستند. به دلیل نیروهای ضعیف تری که ذرات خود را در کنار هم نگه می دارند، مایعات با شکل ظرف خود منطبق می شوند. با این حال، برهمکنش آنقدر قوی است که ذرات را به سمت یکدیگر جذب کند. در نتیجه، مایعات تراکم ناپذیر هستند. این بدان معناست که مایعات تا زمانی که دما و فشار ثابت نگه داشته شوند، حجم ثابتی دارند (بدون توجه به شکل ظرفشان). از آنجایی که حرکت ذرات بیشتر از یک جامد است، مایعات دارای ارزش انرژی جنبشی بالاتری هستند.
هنگامی که جامدات از نقطه ذوب خود عبور می کنند، می توانند انرژی حرارتی را جذب کنند که باعث حرکت ذرات می شود. هنگامی که انرژی کافی برای تضعیف نیروهایی که آنها را ثابت نگه میدارند وارد سیستم شود، ذرات با انتقال به حالت مایع اجازه حرکت بیشتری خواهند داشت. برخی از خواصی که هنگام تحقیق در مورد مایعات باید به آنها توجه کرد عبارتند از شناوری، کشش سطحی، سیالیت و چگالی.

گازها
در حالت گازی، ذرات آزادی حرکت بیشتری نسبت به مایع دارند. در اینجا، ذرات می توانند بدون جذب یکدیگر در جهت های تصادفی حرکت کنند. مولکولها انرژی جنبشی کافی دارند که نیروهای بین مولکولی که آنها را در کنار هم نگه میدارند ناچیز است، که دلیل بر میزان حرکت آنهاست. گازها نیز مانند مایعات شکل مشخصی ندارند. بنابراین، آنها نیز با شکل ظرف خود مطابقت دارند. با این حال، بر خلاف مایعات، گازها قابل تراکم هستند – حجم ثابتی ندارند. این بدان معنی است که ذرات گاز برای پر کردن ظرفی که در آن قرار دارند پخش می شوند. به دلیل فاصله بین ذرات گاز، معمول است که یک گاز بی رنگ برای چشم انسان نامرئی باشد. به همین دلیل است که ما راه هایی برای تشخیص گازها داریم، مانند آشکارسازهای مونوکسید کربن!
با توجه به خواص این حالت ماده، تجزیه و تحلیل ریاضی گازها می تواند دشوار باشد. به همین دلیل است که قانون گاز ایده آل وجود دارد که شرایطی را برای نحوه عملکرد یک گاز در شرایط “عالی” تعیین می کند. همچنین روابط ریاضی مختلفی وجود دارد که شرایطی را برای رفتار گازها ایجاد می کند مانند قانون بویل، قانون چارلز، قانون گی-لوساک، قانون هنری، قانون گاز ترکیبی و قانون آووگادرو.

گازهای خالص در مقابل مخلوط گاز
یک گاز خالص میتواند از اتمهای منفرد (مثلاً گازهای نجیب مانند نئون و آرگون)، مولکولهای عنصری با یک نوع اتم (مثلاً گازهای دو اتمی مانند O) تشکیل شود.2 و N2) یا مولکول های ترکیبی با انواع اتم های متعدد (مثلاً دی اکسید کربن). از طرف دیگر یک مخلوط گاز حاوی انواع گازهای خالص است. یک مثال معمول از مخلوط گاز، هوای جو زمین (که حاوی نیتروژن، اکسیژن، آرگون و چندین گاز دیگر است) است.
پلاسماها
این حالت کمتر شناخته شده ماده زیر مجموعه ای از گازها است. مشابه گازها، پلاسماها شکل یا حجم مشخصی ندارند و چگالی کمتری دارند. باز هم، این بدان معنی است که ذرات با شکل و حجم ظرفی که در آن نگهداری می شوند مطابقت خواهند داشت. با این حال، در حالی که گازها از مولکول هایی با بار خالص صفر ساخته شده اند، پلاسما از ذرات باردار تشکیل شده است. آنها متشکل از دریایی آزادانه از الکترون ها با هسته های دارای بار مثبت “شناور” هستند. در نتیجه، پلاسما می تواند بارهای الکتریکی را هدایت کند و با دیگر نیروهای الکترومغناطیسی تعامل کند.
پلاسما می تواند به یکی از دو روش تبدیل به گاز شود. اول، قرار گرفتن در معرض یک اختلاف ولتاژ بزرگ (برابر یا بیشتر از اختلاف بار 2) بار الکتریکی را از بین می برد و آن را یونیزه می کند و به آن بار خنثی یک گاز می دهد. دوم، با قرار دادن پلاسما در شرایط دمای بالا، الکترون ها از اتم ها خارج می شوند و در نتیجه الکترون های آزاد ایجاد می شود. از آنجایی که فقط برخی از الکترون ها آزاد هستند، این پلاسمای یونیزه شده جزئی نامیده می شود. در برخی شرایط شدید، می توان فرض کرد که همه الکترون ها آزاد هستند. به این پلاسمای کاملا یونیزه می گویند.

نمونه هایی از پلاسما
پلاسما تقریباً 99 درصد از کیهان را تشکیل می دهد. به شکل ستاره ها، سحابی ها و شفق ها می درخشد. علاوه بر این، لایه ای از جو زمین که به یونوسفر معروف است، پلاسما در نظر گرفته می شود. رعد و برق در آسمان و تابلوهای نئونی در خیابان های شهر نمونه های دیگری از پلاسما هستند.
نمونه هایی از حالت های میانی ماده
میعانات بوز-انیشتین (BEC)
در سال 1995، دانشمندان یک حالت انسان ساخت ماده را نشان دادند: میعانات بوز-انیشتین. گروهی از اتم ها هستند که تا نزدیک صفر مطلق (273.15- درجه سانتیگراد) سرد شده اند. در این دما، اتم ها انرژی آزاد برای حرکت نسبت به یکدیگر ندارند. بنابراین، آنها شروع به ادغام در یک حالت کوانتومی واحد می کنند و یکسان می شوند و مانند یک اتم رفتار می کنند. میعانات بوز-اینشتین نقش مهمی در توسعه لیزرهای کم مصرف و سوئیچ های نوری فوق سریع دارند.
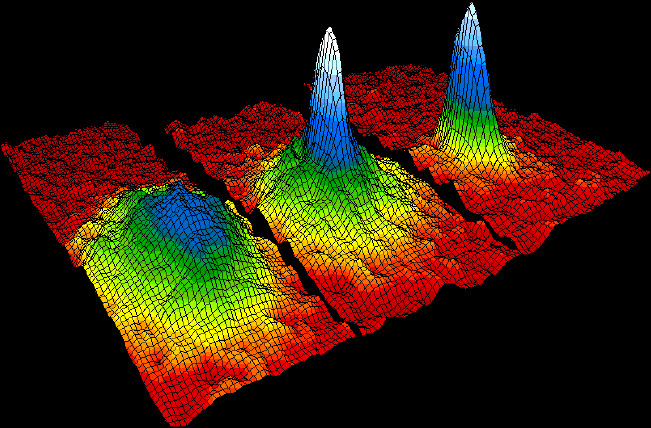
میعانات شیشه ای رنگی
این نوع ماده یک نظریه دارد! ظاهراً در درون هستههای اتم وجود دارد که در حین حرکت نزدیک به سرعت نور با هم برخورد میکنند. در ارتباط با نظریه نسبیت انیشتین، یک هسته با انرژی بالا می تواند فشرده به نظر برسد. در نتیجه، گلوئون ها درون هسته به صورت دیواری ظاهر می شود که با سرعت نور حرکت می کند. چگالی دیواره گلوئون می تواند افزایش یابد و ماده گلوئون اشباع شده به عنوان میعان شیشه رنگی شناخته می شود. این حالت ماده مهم است زیرا به عنوان شکل جهانی ماده برای تجزیه و تحلیل و توصیف خواص ذرات پرانرژی و شدیداً متقابل پیشنهاد شده است.
